Как получить перекись водорода

Твердый электролит помог напрямую синтезировать перекись водорода
Перекись водорода пероксид водорода , H2O2 — простейший представитель пероксидов. Бесцветная жидкость с «металлическим» вкусом, неограниченно растворимая в воде, спирте и эфире. Концентрированные водные растворы взрывоопасны. Пероксид водорода является хорошим растворителем.





Американские химики разработали систему прямого электрохимического синтеза раствора пероксида водорода концентрацией до 20 процентов из водорода и кислорода. С помощью электрохимической ячейки из платиноуглеродного анода, катода из технического углерода и твердого электролита между ними авторам статьи, опубликованной в Science , удалось раздельно окислить водород и восстановить кислород, после чего в потоке воды ионы в твердом электролите образовывали пероксид водорода. Полученный раствор оказался достаточной чистоты, чтобы использовать его непосредственно из устройства.
- Смотрите также
- Ученые обнаружили, что перекись водорода H 2 O 2 может самопроизвольно образовываться на поверхности небольших водяных капель, что противоречит распространенному мнению о стабильности и химической инертности воды.
- Концентрированные водные растворы взрывоопасны.
- Пероксид водорода H 2 O 2 - это очень популярное неорганическое химическое соединение.
- Содержание
- Воздух, вода и электричество: ученые из Массачусетского технологического университета усовершенствовали антрахиноновый процесс. Пероксид перекись водорода — препарат, используемый для обеззараживания ран и поверхностей, а также как обесцвечивающее средство.
- Перекись водорода медицинскую H2О2 водорода пероксид, пергидроль применяют в химической, целлюлозно-бумажной, текстильной, медицинской и в бассейнах. Для стабилизации перекиси водорода медицинской применяют дифосфат натрия или однозамещенный фосфорнокислый натрий.
- Effective date :
- Для продолжения работы вам необходимо ввести капчу
- Относительно высокая вязкость жидкого пероксида водорода обусловлена развитой системой водородных связей.
- Противомикробный компонент. Проникают в эмаль и выделяет активный кислород, за счёт чего происходит окисление пигментированного дентина.
- Просмотров , рейтинг 3. В данном материале хочу поделится простым и доступным средством для изготовления перекиси водорода в домашних условиях.









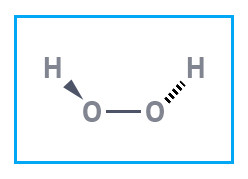
Удобная навигация, видео-разборы тем, задачи для самопроверки — всё это в вашем кармане. А ещё раздел с полезными материалами, календарь занятий и уведомления о предстоящих уроках. Строение перекиси водорода. В молекуле пероксида водорода содержится группировка атомов , называемая пероксидной. У каждого атома кислорода в этом соединении степень окисления равна. Связь непрочна, поэтому пероксид водорода и его концентрированные растворы самопроизвольно разлагаются на свету со взрывом.